داروهای مسکن به دو نوع داروهای مسکن_خواب آور و داروهای مسکن_تب بر تقسیم میشوند:
داروهای مسکن_خواب آور
انواع داروهای مسکن_خواب آور داروهای مضعف عمومی یا غیر انتخابی سیستم اعصاب مرکزی هستند. این مواد برای کاهش بیقراری و تنشهای هیجانی و همچنین برای تسکین و یا ایجاد خواب به کار میروند. تمایز میان آثار تسکینی و خواب آوری کاملا مشخص نیست. یک داروی واحد میتواند بسته به روش مصرف و مقدار بکار رفته هر دو اثر را بروز دهد مقدار اندک تنها سبب تسکین میشود حال آنکه مقادیر بیشتر سبب اثر خواب آوری میگردد. برخی از این داروها در مقادیر زیاد برای ایجاد بیهوشی در جراحی یا به عنوان بیهوش کننده فرعی به کار میروند.
ترکیبات مسکن-خواب آور از نظر ساختمان شیمیایی تفاوت زیادی دارند اگر چه عوامل مفید در چند دسته شیمیایی متفاوت یافت شدهاند اما دارای چندین جنبه فیزیکوشیمیایی و ساختمانی مشترک نظیر یک ناحیه قطبی آبدوست، ضریب توزیع اکتانول- آب نزدیک به 100 و مقاومت زیاد در برابر تغییرات زیستی میباشند.
انواع داروهای مسکن_خواب آور
ترکیبات متداولی که اغلب بعنوان داروی مسکن_خواب آور مورد مصرف قرار میگیرند وابسته به یکی از گروههای زیر میباشند:
بنزودیازپینها، باربیتواتها، پیریدین دیونها و تریونها، مشتقات کینازولین، الکلها، کارباماتها، آلدئیدها و مشتقات آنها، آمیدها، شبه اورههای غیر حلقوی، بنزآزپینها و داروهای وابسته، فتوتیازینها، مواد درونزای مربوط به خواب و عوامل متفرقه.
نحوه عملکرد داروهای مسکن- تب بر
داروهای مسکن- تب بر همچنین تحت عنوان مقابله کنندگان با درد نیز شناخته شدهاند زیرا باعث تخفیف حساسیت نسبت به درد که توسط پروستاگلاندینها القا میشود، میگردند. این ترکیبات حالت حساسیت نسبت به درد (آستانه پایین درد) را به آستانه درد عادی بر میگردانند. اگرچه برخی دارای خواص ضد التهابی نیز هستند، اما فعالیت ضد دردی آنها مستقل از این خصوصیات است. این ترکیبات، آثار خود را به صورت موضعی در محل یا نزدیکی محلی که مشکل ایجاد شده است، اعمال میکنند که بر آثار مرکزی ارجحیت دارد.
اعتقاد بر اینست که نحوه اثرشان از طریق مهار انتخابی از آنزیم ها (مثل سیکلو اکسیژناز) است که بیوسنتز پروستاگلازین ها را کاتالیز میکنند. مهار این آنزیم ها از حساسیت گیرندههای درد نسبت به میانجیها و تنظیم کنندههای درد، ادراک، تحریکهای مکانیکی یا مواد شیمیایی مانند یونها (مثل هیدروژن و پتاسیم)،هیستامین، سروتونین، ماده p، پرسوتاسیکلین و پرسوتاگلاندینها جلوگیری به عمل میآورد.
با این حال اثر درمانی این داروها میتواند به عوارض ناخواسته ناشی از آنها نیز مرتبط باشد: تحریک دستگاه گوارش و ایجاد زخم، مهار به هم چسبیدن پلاکتهاو افزایش زمان خونریزی، کاهش عملکرد کلیوی و علائم حساسیتی.
اولین اثر آسپیرین، غیر فعال کردن سیکلواکسیژناز از طریق استیله کردن برگشت ناپذیر دنباله سرین این آنزیم که جزیی از کمپلکس چند آنزیمی به نام پروستاگلاندین سنتتاز یا آنزیمی است که مرحله اول سنتز زیستی پروستاگلاندین از اسید آراشیدونیک را کاتالیز میکند، میباشد.
اسید سالیسیلیک فاقد این فعالیت استیله کنندگی است بنابراین نحوه عملکرد آن باید متفاوت باشد.
__عوارض ناخواسته داروهای مسکن- تب بر
عمدهترین عوارض نامطلوب اغلب داروهای مسکن تب بر، تحریک دستگاه گوارش و ایجاد زخم، کاهش فعالیت کلیوی، مهار انعقاد پلاکتی و در نتیجه افزایش مدت خونریزی و علائم حساسیتی است. مصرف طولانی مدت این ترکیبات سبب بیماری کلیوی "nephropathy" میگردد.
دیدکلی
تومورهای پوستی در قسمتهای مختلف بدن روی صورت ، گردن ، بالای قفسه سینه و پشت ظاهر میشود که اغلب تومورها به صورت کیستهای موئی هستند که به آنها کیستهای سبابه گفته میشود که بیشتر روی پوست مشاهده میشوند. از بخش میانی فولیکول مو و سلولهای پوشش خارجی ریشه مو نشات میگیرند.
درمان آنها با جراحی و برداشتن تمام کیست یا توده انجام میشود. این تودهها میتوانند به صورت ضایعاتی باشند که آنها را به دو قسمت اولیه و ثانویه تقسیم کردهاند. تومورهای اولیه از ابتدای بیماری وجود داشته ولی تومورهای ثانویه به علت عوامل بیرونی مثل خراشیدگی ، تروما و عفونت ایجاد میشوند. اکثر این تومورهای پوستی ، خوش خیم هستند.
انواع تومورهای اولیه
- ماکول :
تغییر رنگ پوست با حدود واضح بدون برجستگی. - پاپول :
ضایعه برجسته و توپر پوست به قطر کمتر از یک سانتیمتر که ممکن است رنگهای گوناگونی داشته باشد. - ندول :
ضایعه برجسته توپر به قطر بیشتر از یک سانتیمتر. - وزیکول :
بر آمدگی کوچک پوستی که از مایع شفاف پر شده است. - بول (تاول) :
وزیکول بزرگ به قطر بیشتر از یک سانتیمتر. - پرستول :
ضایعهای حاوی چرک که ممکن است ناشی از تغییرات چرکی در وزیکول باشد. - کهیر :
برآمدگی موقت پوست به علت ادم درم و گشاد شدن مویرگهای اطراف آن. - پلاک :
ضایعه برجسته و توپر پوست به قطر بیش از یک سانتیمتر. - کسیت :
تومور حاوی ماده جامد یا مایع.
انواع تومورهای ثانویه
- پوسته :
لایههای جدا شده طبقه شاخی پوست که ممکن است در اثر تغییرات التهابی بوجود آیند. - کراست (دلمه) :
لایهای مرکب از سرم ، خون یا چرک خشک شده در روی پوست. - خراشیدگی :
خطوط خراشیدگی یا ضربه دیدگی. - فسیور :
ترک خوردگی پوست که معمولا در اثر خشکی شدید و التهاب طولانی است. - بافت جوشگاه :
تغییر فیبروتیک پوست به دنبال فرآیند تخریبی. - لیکنی شدن :
ضخیم شدن پوست و مشخص تر شدن چینهای پوستی.
انواع تومورهای خوش خیم
کواتوزهای سبورهای
تومورهای خوش خیم و زگیل مانند با اندازهها و رنگهای مختلف از قهوهای روشن تا سیاه مشاهده میشوند. روی صورت ، شانه ، قفسه سینه و پشت بوجود میآیند و شایع ترین تومورهای پوست هستند. درمان این تومور بوسیله روشهای جراحی (اکسیزیون) ، کرتریزاسیون و کورتاژ ، یا مالیدن دی اکسید کربن یانیتروژن مایع انجام میشود.
کراتوزهای اکتنیک
ضایعاتی در نواحی باز پوست پس از تماس طولانی با آفتاب بوجود میآید، ممکن است به ضایعاتی بد خیم تبدیل شود (10 تا 20 درصد به سرطان مهاجم سلول اسکواموس تبدیل میشوند) که به شکل لکههای پوسته زبر ، روی زمینه اریتم تظاهر میکند.
زگیل
در اثر عفونت ، ویروس یا پیلومای انسانی ، متعلق به گروه ویروسهای DNA دار ایجاد میشود که اصولا فاقد علامت هستند. مگر آن که در قسمتهایی از پوست بدن که وزن را تحمل میکند (مثل کف پا) ظاهر شوند. زگیل را میتوان با اشعه لیزر ، نیتروژن مایع ، اسید سالیسیک کرتریزاسیون یا مالیدن کانتاریدینبرطرف نمود.
 |
ساختمان شیمیایی انسولین
انسولین پلیپپتیدی است که از دو زنجیره پپتیدی A و B تشکیل یافته است. تعداد اسیدهای آمینه در زنجیرهها که در زنجیره A برابر 21 و در زنجیره B برابر 30 میباشد، در انسولینهای جدا شده از اغلب گونههای حیوانی ثابت است. این دو زنجیره به کمک دو پل دیسولفور ، یکی بین اسیدهای آمینه شماره 7 از دو زنجیره و دیگری میان اسیدهای آمینه شماره 20 از زنجیره A و شماره 19 از زنجیره B با یکدیگر اتصال دارند. علاوه بر این ، ریشههای اسید آمینه ردیف 6 و 11 در داخل زنجیره A بوسیله پیوند دیسولفور به یکدیگر متصل هستند. مکان این پیوندها در گونههای مختلف ، ثابت است.
پژوهشگران با بررسی اثرات تغییرات شیمیایی هر یک از اسیدهای آمینه در ردیفهای مختلف ساختمان انسولین موفق شدهاند، قسمتهایی از ساختمان انسولین را که برای بروز اثرات زیست شناختی آن ضروری هستند را تعیین کنند. انسولین در غلظتهای فیزیولوژیک به صورت یک مونومر ساده میباشد و در غلظتهای بالاتر ، انسولین پلیمریزه شده و ساختمان کمپلکس را به خود میگیرد و یونهای روی (Zn ) نقش بسیار مهمی را در ایجاد این کمپلکس بر عهده دارند.
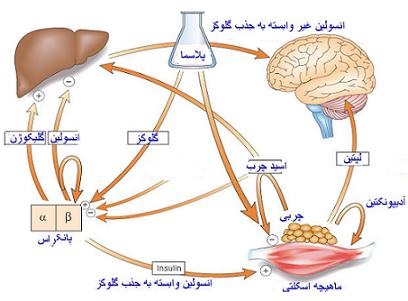
سیستم تنظیم ترشح انسولین
اثر گلوکز
افزایش گلوکز خون ، مهمترین عامل فیزیولوژیک تنظیم کننده ترشح انسولین است. غلظت گلوکز خون در حالت ناشتا (80 - 100 میلی گرم درصد) آستانه غلظتی است که تجاوز از آن با تحریک ترشح انسولین همراه است. و بیشترین اثر محرک گلوکز زمانی حاصل میشود که غلظت آن در خون به حدود 500 - 300 میلیگرم درصد برسد.
 |
| عملکرد انسولین |
اثرات انسولین در متابولیسم گلوکز
انسولین با افزایش کمی و همچنین افزایش فعالیت تعدادی از آنزیمهای کلیدی در واکنشهای گلیکولیز کبدی مانند آنزیمهای گلوکوکیناز و پیروات کیناز، مصرف گلوکز در مسیر گلیکولیز را افزایش داده و بطور غیرمستقیم از رها شدن گلوکز در پلاسمای خون جلوگیری میکند. از سوی دیگر ، انسولین با کاهش فعالیت آنزیم گلوکز 6- فسفاتاز موجود در کبد از آزاد شدن گلوکز جلوگیری میکند. چون گلوکز 6- فسفات قادر به عبور از غشا سلول کبدی نیست، عمل انسولین منجر به نگهداری گلوکز در داخل سلولهای کبدیمیشود.
یکی دیگر از اثرات انسولین که منجر به کاهش غلظت گلوکز در پلاسما میگردد، اثراتی است دیررس که در نتیجه مهار کردن واکنشهای نوسازی گلوکز حاصل میگردد. مهمترین آنزیم کلیدی در واکنشهای نوسازی گلوکز از مواد غیر قندی در کبد آنزیم فسفوانول پیروات کربوکسی کیناز میباشد که واکنش تبدیل شدن اگزالواستات به فسفوانول پیروات را کاتالیز میکند. انسولین با ویژگی خاص ، اثر بازدارنده در رونویسی ژن این آنزیم داشته و از سنتز RNA پیامبر مربوط به آن ، جلوگیری میکند.
اثر انسولین در متابولیزم چربیها
در بافتهای کبدی و چربی ، انسولین دارای اثر بازدارنده قوی در واکنشهای لیپولیز (تجزیه چربیها) است که این اثر نیز خود بطور غیر مستقیم به اثرات آنابولیسمی میانجامد. اثر بازدارنده انسولین در واکنشهای لیپولیز از دو راه صورت میگیرد. در حالیکه هورمونهای محرک واکنشهای لیپولیز یعنی گلوکاگن و اپی نفرین عمل خود را از طریق افزایش غلظت AMP حلقوی به انجام میرسانند، انسولین با اثری مخالف موجب کاهش غلظت AMP حلقوی میگردد. انسولین با فعال ساختن یک آنزیم فسفاتاز ویژه ، از فعالیت آنزیم لیپاز ، که در تجزیه چربیها نقش دارد جلوگیری مینماید. اثر بازدارنده انسولین در واکنشهای لیپولیز به کاهش غلظت اسیدهای چرب آزاد در جریان خون و نهایتا به افزایش اثرات انسولین در متابولیسم گلوکز میانجامد.
اطلاعات اولیه
قبل از هر چیز باید بدانیم که آیا ویروسها موجودات زنده محسوب میشوند یا نه. یک تعریف میگوید: حیات عبارت است از یکسری فرایندهای پیچیده حاصل از دستورالعملهای خاصی که بوسیله اسید نوکلئیک سلولهای زنده همواره در فعالیت میباشد. چون ویروسها در خارج از بدن میزبان به حالت خنثی بسر میبرند به این مفهوم نمیتوان آنها را موجود زنده در نظر گرفت. معهذا هنگامی که ویروسها وارد سلول میزبان میشوند اسیدهای نوکلئیک آنها فعال گشته و منجر بهتکثیر ویروس میگردد. از نظر بالینی ویروسها را میتوان موجودات زنده در نظر گرفت زیرا آنها مانند باکتریها ، قارچهای بیماریزا آلودگی و بیماری ایجاد میکنند. به ویروس کامل ویریون گفته میشود.
ساختمان شیمیایی ویروس
اسید نوکلئیک
یک ذره ویروسی دارای یک هسته مرکزی اسید نوکلئیکی DNA یا RNA به عنوان ماده ژنتیکی میباشد. نسبت اسید نوکلئیک به پروتئین غلاف ویروس از یک درصد در ویروس آنفلوانزا تا 50 درصد در برخی از باکتریوفاژها متغیر است. برخلاف سلولهای پروکاریوتیک و یوکاریوتیک که همواره دارای DNA به عنوان ماده ژنتیکی اصلی خود هستند ویروسها دارای یکی از دو نوع اسید نوکلئیک بوده و هرگز هر دو را باهم ندارد. اسید نوکلئیک در بعضی ویروسها به شکل خطی و در بعضی به شکل حلقوی میباشد.
کپسید
اسید نوکلئیک ویروس بوسیله غلاف پروتئینی به نام کپسید احاطه شده است. کپسید ویروس که معماری آن بوسیله اسید نوکلئیک ویروسی تعیین میشود بخش عمده ویروس را بویژه در ویروسهای کوچک شامل میشود. هر کپسید از واحدهای کوچک پروتئینی به نام کپسومر ساخته شده است. نظم و ترتیب قرار گرفتن کپسومرها ، شکل کلی و پیکر ویروس را تعیین میکند که برای هر ویروس خاص ثابت است.
پوشش غیر پروتئینی
در عدهای از ویروسها کپسید بوسیله پوششی که معمولا ترکیبی از لیپیدها ، پروتئینها و کربوهیدراتها است پوشیده شده است.
در بیماریهای مختلف مقدار هورمونها در خون افزایش یا کاهش مییابد. پزشک میتواند این گونه بیماریها را با دانستن مقدار یک هورمون در خون تشخیص دهد. از این رو، پس از معاینهی بیمار اگر برخی از نشانههای بیماری هورمونی را در او تشخیص دهد، بررسی هورمونی را به بیمار پیشنهاد میکند. بیمار به آزمایشگاه تشخیص طبی مراجعه میکند و در بخش هورمونشناسی از او مقداری خون میگیرند و با کمک ابزارها و روشهای زیستشیمیایی میزان هورمونها در خون وی اندازه گیری میشود.
سنجش رادیوایمنی:
اصول سنجش رادیوایمنی از این قرار است:
1. مقدار زیادی پادتن برای هورمون مورد نظر تهیه میشود.
2. مقداری هورمون خالص با ایزوتوپ رادیو اکتیو نشاندار میشود.
3. مقداری از پلاسمای خون فرد مورد نظر با پادتن هورمون و مقدار مشخصی هورمون نشاندار مخلوط میشود.
در این مخلوط، هورمون موجود در پلاسما با هورمون نشاندار بر سر اتصال به پادتن با هم رقابت میکنند. در این رقابت مقدار هر کدام از هورمونها(غیر نشاندار و نشاندار) با غلظت آنها متناسب است. اما مقدار پادتن باید کمتر از آن باشد که تمام هورمون نشاندار و هورمون غیر نشاندار به آن متصل شوند.
4. پس از آنکه رقابت به پایان رسید، مجتمع "هورمونپادتن" از بقیهی مخلوط جدا و مقدار هورمون رادیواکتیو با دستگاه رادیو اکتیوسنج اندازهگیری میشود.
اگر مقدار رادیواکتیو سنجششده بالا باشد، نشان میدهد مقدار زیادی هورمون نشاندار به پادتنها متصل شده است. بنابراین مقدار اندکی هورمون غیر نشاندار با هورمون نشاندار رقابت کرده و بنابراین غلظت هورمون غیر نشاندار در پلاسمای مورد سنجش کم بوده است.
اگر مقدار رادیواکتیو سنجش شده پایین باشد، نشان میدهد مقدار اندکی هورمون نشاندار به پادتنها متصل شده است. بنابراین مقدار زیادی هورمون غیر نشاندار با هورمون نشاندار رقابت کرده و بنابراین غلظت هورمون غیر نشاندار در پلاسمای مورد سنجش زیاد بوده است.
5. برای این که اندازهگیری از حالت کیفی به حالت کمی (مقداری) تبدیل شود، رادیو ایمنی با غلظتهای مختلف اما مشخصی از هورمون غیر نشاندار انجام میشود. آنگاه منحنی استانداردی تهیه میشود که با داشتن آن میتوان غلظت یک هورمون را به طور دقیق مشخص کرد.
امروزه همهی مواد لازم برای انجام رادیوایمنی جهت سنجش هورمونها در بستهبندیهای ویژهای به نام "کیت" در اختیار آزمایشگاهها قرار میگیرد. چگونگی بهرهگیری از کیت و در واقع چگونگی انجام رادیوایمنی در دفترچهی راهنمای آن آمده است.
1. پادتن هورمون مورد نظر به ته لولههای ویژه متصل است.
2. هورمون نشاندار و هورمون غیر نشاندار به لولهها افزوده میشوند.
3. دو هورمون برای اتصال به پادتن رقابت میکنند. هورمونهایی که متصل نشدهاند شسته میشوند.
4. مقدار هورمون نشاندار با دستگاه تعیین و غلظت هورمون غیر نشاندار بر پایهی آن محاسبه میشود.
سنجش ایمنیآنزیم: ELISA
این روش تفاوت بنیادی با سنجش رادیوایمنی ندارد. فقط در این روش به جای مادهی رادیواکتیو از فعالیت آنزیمی بهره گرفته میشود. به عبارت دیگر، به جای هورمون نشاندار ، هورمونی به کار میرود که به آنزیم پراکسیداز متصل است. در صورتی که سوبسترا(ماده واکنشگر)ی این آنزیم در محیط باشد، این آنزیم آن را به فرآوردهی رنگینی تبدیل میکند. با روش رنگسنجی میتوان مقدار فرآوردهی تولید شده و به عبارتی میزان هورمون نشاندار را تعیین کرد. در سنجش ایمنیآنزیم نیز تعیین مقدار هورمون در نمونهی پلاسما به کمک منحنی استاندارد انجام میشود.
توجه: در این جا اصول کلی سنجش هورمونها بیان شد. جزپیات این کار بر پایهی نوع هورمون یا شیوهی ابداعی شرکتی که کیت را تولید میکند ، ممکن است اندکی تفاوت داشته باشد.
مقدار هورمونها و علت شناسی بیماریها
در اینجا با یک مثال میخواهیم شرح دهیم که دانستن مقدار هورمونها چگونه به پزشک در تشخیص علت بیماری کمک میکند.
همان گونه که میدانید غده هیپوفیز فعالیت بیشتر غدههای هورمونی را تنظیم میکند. این غده با رهایی هورمونهایی به نام هورمونهای تحریککننده به درون خون باعث ترشح هورمونهای دیگری از سایر غدهها میشود. برای مثال، هورمون تیروئیدی TSH با اثر بر غدهی تیروئید باعث افزایش ترشح هورمونهای تیروییدی( T3 و T4 ) از این غده میشود. از سوی دیگر، فعالیت ترشحی خود غده هیپوفیز در نظارت بخشی از مغز به نام هیپوتالاموس است. هیپوتالاموس با رهایی هورمونهایی به نام هورمونهای آزادکننده یا بازدارنده باعث ترشح یا مانع ترشح هورمونهای تحریککننده از هیپیوفیز میشود. برای مثال، هورمون هیپوتالاموسی TRH باعث رهایی TSH از هیپوفیز میشود. سپس TSH با اثر بر غدهی تیروئید بر ترشح T3 و T4 از این غده میافزاید. در حالت عادی وقتی میزان T3 و T4 در خون افزایش مییابد این هورمونها با اثر روی هیپوفیز و هیپوتالاموس از میزان ترشح TSH و TRH از غدههای مربوط، میکاهند و به طور غیرمستقیم مانع افزایش بیش از اندازهی خود میشوند.
حال بیماری را در نظر بگیرید که نشانههای پرکاری تیروئید در او دیده شده است. آیا این بیمار به علت اختلال در کارکرد غدهی تیروئید به این عارضه دچار شده یا بیماری او به علت افزایش ترشح TSH از غدهی هیپوفیز است؟ اندازهگیری هورمونهای تیروئید( T3 و T4 ) و TSH میتواند به علتشناسی بیماری کمک کند.
• اگر مقدار هورمونهای تیروئیدی(T3 و T4) در خون بالا باشد و مقدار TSH پایین باشد، نشاندهندهی این است که پرکاری تیروئید به علت اختلال در خود تیروئید رخ داده است. برای مثال، در بیماری گریوز(Graves) که مهمترین عامل پرکاری تیروئید است، به علت واکنشهای خودایمنی پادتنی علیهی گیرنده TSH (در سطح سلولهای غدهی تیروئید) ساخته میشود. این پادتن باعث تحریک این گیرنده و افزایش تولید و ترشح هورمونهای تیروئید میشود. با افزایش هورمونهای تیروئیدی مقدار TSH کاهش مییابد. از این رو، در این بیماران مقدار T3 و T4 بالا و مقدار TSH پایین است. تعیین مقدار پادتن ضد گیرندهی TSH علتشناسی را اصمینانبخشتر میکند.
• اگر مقدار هورمونهای تیروئیدی و مقدار TSH نیز بالا باشد، ممکن است پرکاری تیروئید به علت اختلال در هیپوفیز رخ داده باشد. سرطانیشدن هیپوفیز یا مقاومت آن به هورمونهای تیروئیدی باعث افزایش ترشح TSH میشود. TSH با تحریک غدهی تیروئید مقدار ترشح T3 و T4 را افزایش میدهد.(منظور از مقاومت هیپوفیز به هورمونهای تیروئید این است که این غده در پاسخ به افزایش T3 و T4 مقدار ترشح TSH را کاهش نمیدهد.)
یک مثال واقعی
خانمی 16 ساله به علت پوسته پوسته شدن پوست، رکود رشد موها، خستگی و خوابآلودگی شدید و اندکی گرفتگی صدا به پزشک مراجعه کرد.
معاینهی پزشک:
1. کاهش تعداد ضربان قلب واضح است.
2. همیشه احساس سرما دارد.
3. زیر چشمها پفآلود است.
4. برونده قلب و حجم خون کاهش یافته است.
بررسی آزمایشگاه :
1. T3 و T4 ، بالا
2. TSH ، بالا
3. TRH ، پایین
4. بررسی هیپوفیز، طبیعی
چون مقدار هورمونهای تیروئید در این بیمار بالاست، وی باید نشانههای پرکاری تیروئید(از جمله افزایش ضربان و برونده قلب و احساس گرما و تعرق زیاد) را نشان دهد، اما برعکس نشانههای کاهش فعالیت تیروئید را نشان میدهد.
به نظر میرسد در این بیمار سلولهای بدن به دلایل ژنتیکی یا عارضهای به هورمونهای تیروئیدی پاسخ نمیدهند. در نتیجه در این بیمار با وجود بالا بودن T3 و T4 نشانههای کمکاری تیروئید دیده میشود. چون مقدار هورمونهای تیروئیدی بالاست، انتظار میرود مقدار TSH پایین باشد اما به نظر میرسد مقدار TSH به علت مقاومت هیپوفیز به هورمونهای تیروئیدی افزایش یافته است.
.: Weblog Themes By Pichak :.
